ویژگیها
نوشتار اصلی: فلزهای قلیایی
لیتیوم فلز نایابی نیست. میزان لیتیوم موجود در پوسته زمین برابر با ۰،۰۰۶ درصد است که بنظر کم میآید اما همین اندازه نیز از موجودی فلزات دیگر مانند قلع و جیوه بیشتر میباشد.
تنها فرقی که میان لیتیوم و دیگر فلزها وجود دارد، وضعیت پراکندگی آن بر روی کره زمین است.
نخست آنکه مکانهایی که لیتیوم در آنجا گرد آمدهاست زیاد نیستند. منابع قابل توجه و شناخته شده لیتیوم بر روی زمین شیلی، آرژانتین، تبت، چین، ایالت نوادای آمریکا و بولیوی میباشند.
این در حالیست که منابع بولیوی که معدن شناسان میزان ذخایرش را برابر با ذخایر افغانستان تخمین میزنند، هنوز آغاز به بهره برداری نکردهاست.
فیزیکی و اتمی
مانند دیگر فلزهای قلیایی، لیتیم تنها یک الکترون در لایهٔ ظرفیت دارد که دوست دارد آن را به آسانی از دست دهد و تبدیل به کاتیون شود.[۱] به همین دلیل لیتیم یک رسانای خوب گرما و جریان برق است و واکنش پذیری بسیار بالایی دارد. با این وجود از نظر واکنش پذیری در میان فلزهای قلیایی رتبهٔ آخر را دارد. این واکنش پذیری کم نسبت به دیگر عنصرهای گروه، به دلیل نزدیکی زیاد الکترونهای لایهٔ ظرفیت به هستهٔ اتم لیتیم است. چون دو الکترون باقی مانده در تراز ابر الکترونی 1s جای میگیرند که تراز انرژی بسیار پایینی دارد برای همین در پیوندهای شیمیایی شرکت نمیکنند.[۱]
فلز لیتیم آنقدر نرم است که با چاقو بریده شود. هنگامی که بریده شد یک سطح نقرهای-سفید از آن دیده میشود. این رویه خیلی زود اکسید میشود و به رنگ خاکستری در میآید.[۱] لیتیم دارای یکی از پایین ترین نقطهٔ ذوبها (180 °C) در میان همهٔ فلزها است در حالی که در میان فلزهای قلیایی، بالاترین نقطهٔ ذوب و جوش را دارد.[۲]
لیتیم سبک ترین فلز جدول تناوبی است با چگالی نزدیک به ۰٫۵۳۴ g/cm۳ و یکی از سه فلزی است که روی آب و حتی روغن، شناور میماند (دو فلز دیگر سدیم و پتاسیم]] است).[۱] لیتیم کم چگالی ترین عنصری است که در دمای اتاق گاز نیست. سبک ترین عنصر پس از لیتیم، پتاسیم است که بیش از ۶۰٪ آن (۰٫۸۶۲ g/cm۳) چگالی دارد. همچنین اگر هلیم و هیدروژن را کنار بگذاریم، لیتیم کم چگالی ترین عنصر در میان دیگر عنصرهای جامد و مایع است. برای نمونه لیتیم تنها ۲/۳ نیتروژن مایع (0.808 g/cm۳) چگالی دارد.[note ۱][۳]
ضریب انبساط گرمایی لیتیم دو برابر آلومینیم و نزدیک به چهار برابر آهن است.[۴] می توان گفت لیتیم دارای بالاترین ظرفیت گرمایی در میان همهٔ عنصرهای جامد است. لیتیم در فشار معمولی، در دمایی پایین تر از ۴۰۰ μK ابررسانا میشود[۵] و در فشارهای بالا، بیش از ۲۰ گیگاپاسکال، در دمای بیش از ۹ کلوین ابررسانا میگردد.[۶] در دمای زیر ۷۰ کلوین، لیتیم هم مانند سدیم دچار استحاله مارتنزیتی میشود. همچنین در دمای ۴٫۲ کلوین دارای دستگاه بلوری لوزیپهلو (با ۹ لایهٔ فاصلهٔ تکرارشونده) اما در دماهای بالاتر شکل دستگاه بلوری اش به دستگاه بلوری مکعبی وجوهمرکزپُر و سپس به دستگاه بلوری مکعبی مرکزپُر دگرگون میشود. در دمای هلیم مایع (۴ کلوین) ساختار بلوری لوزیپهلو از همه بیشتر دیده شدهاست.[۷] در فشارهای بالا، چندشکلیهای گوناگونی از لیتیم گزارش شدهاست.[۸]
لیتیم به دلیل ظرفیت گرمایی بسیار بالایی که نسبت به دیگر عنصرهای جامد دارد بیشتر در سردکنندهها برای جابجایی گرما به کار گرفته میشود.[۹]
شیمیایی و ترکیبها
لیتیم به سادگی با آب واکنش میدهد ولی انرژی بسیار کمتری نسبت به دیگری فلزهای قلیایی در این واکنش پدید میآید. محصولهای این واکنش گاز هیدروژن و هیدروکسید لیتیم در محلول آبی است.[۱] به دلیل واکنش بالای لیتیم با آب، همواره آن را زیر پوشش هیدروکربنهای گرانرو مانند وازلین نگه میدارند. فلزهای قلیایی سنگین تر را میتوان در مواد با گرانروی پایین تر، مانند روغن صنعتی نگهداری کرد، لیتیم به اندازهٔ کافی سنگین نیست تا بتواند به طور کامل پایین تر از سطح این مایعها قرار گیرد.[۱۰] در هوای مرطوب لیتیم به سرغت اکسید میشود و یک لایهٔ سیاه بر روی آن ساخته میشود. این پوشش سیاه رنگ، هیدروکسید لیتیم (LiOH و LiOH·H۲O)، لیتیم نیتریت (Li۳N) و لیتیم کربنات (Li۲CO۳، نتیجهٔ یک واکنش دوم میان LiOH و CO۲) است.[۱۱]
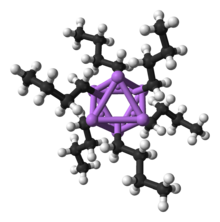
ساختار هشت وجهی بلور ان-بوتیللیتیم
هنگامی که لیتیم در برابر آتش قرار گیرد، ترکیبهای آن رنگ لاکی (قرمز سیر) از خود نشان میدهند اما درصورتی که این ماده آتش گیرد، شعله به رنگ نقرهای در خواهد آمد. هرگاه لیتیم در تماس با آب یا بخار آن، قرار گیرد شعله ور میشود و با اکسیژن میسوزد.[۱۲] لیتیم به خودی خود آتشگیر است و توان انفجار دارد بویژه هنگامی که در هوای آزاد و در تماس با آب قرار گیرد. با این حال این ویژگی لیتیم نسبت به دیگر فلزهای قلیایی، از همه کمرنگ تر است. واکنش لیتیم با آب در دمای معمولی، به تندی صورت میگیرد اما آسیب رسان نیست و هیدروژن تولیدی به خودی خود آتش نمیگیرد. مانند دیگر فلزهای قلیایی، خاموش کردن آتش لیتیم کمی دشوار است و حتما باید از گَردهای خاموش کننده آتش، ردهٔ D کمک گرفت (خاموشکنندههای دستی آتش را نگاه کنید). لیتیم تنها فلزی است که در دمای معمولی و شرایط معمولی با نیتروژن واکنش میدهد.[۱۳][۱۴]
لیتیم یک سری همانندیهای قطری هم با منیزیم دارد. این دو فلز دارای شعاع اتمی و یونی یکسان اند. همانندیهای شیمیایی این دو عبارتند از: ساختن نیترید در اثر واکنش با N۲، ساختن اکسید (Li۲O)) و پراکسید (Li۲O۲) در هنگام سوختن با O۲، پدید آوردن نمکهایی با ویژگی حل شدنی همانند و ناپایداری گرمایی کربنات و نیترید آنها.[۱۱][۱۵] این فلز در دمای بالا با گاز هیدروژن واکنش میدهد و لیتیم هیدرید (LiH) را تولید میکند.[۱۶]
دیگر ترکیبهای دوتایی لیتیم عبارتند از هالیدها (LiF، LiCl، LiBr، LiI) و سولفید (Li۲S)، سوپراکسید (LiO۲)، کربید (Li۲C۲). همچنین شمار بسیاری ترکیبهای غیرآلی هم از این عنصر شناخته شدهاست که در آن لیتیم با یونها آمیخته میشود و نمکهای گوناگونی را پدید میآورد که از آن جمله میتوان به بوراتها، آمیدها، کربنات، نیترات، بوروهیدرید (LiBH۴) و... اشاره کرد. چندین واکنشگر ناب آلی از لیتیم هم شناخته شدهاست که در آنها پیوند کووالانسی مستقیم میان کربن و لیتیم برقرار شده و کربانیون را ساختهاست. اینها بازها و هسته دوستهایی بسیار قوی اند. در بسیاری از ترکیبهای آلی لیتیم، یونهای لیتیم دوست دارند به صورت خوشههای با تقارن بالا روی هم انباشته شوند. میتوان گفت این ویژگی برای کاتیونهای قلیایی معمول است.[۱۷]
ایزوتوپ
نوشتار اصلی: ایزوتوپهای لیتیم
۶Li و ۷Li دو ایزوتوپ پایدار لیتیم و دارای بیشترین فراوانی (۹۲٫۵٪) است.[۱][۱۰][۱۸] این دو ایزوتوپ پایدار در مقایسه با دو عنصر سبک و سنگین همسایگی خود یعنی هلیم و بریلیم، به صورت غیر طبیعی، انرژی پیوستگی هستهای پایینی به ازای هر هسته دارند. به جز دوتریوم و هلیم-۳، دو هستهٔ لیتیم انرژی پیوستگی کمتری به ازای هر هسته، نسبت به هر هستهٔ پایدار دیگری دارند.[۱۹] در نتیجهٔ این پدیده، عنصر لیتیم با اینکه وزن اتمی کمی دارد اما در سامانهٔ خورشیدی از دید فراوانی، در میان ۳۲ عنصر، رتبهٔ ۲۵ ام را دارد.[۲۰] هفت ایزوتوپ پرتوزا برای لیتیم پیدا شدهاست که پایدارترین آنها ۸Li با نیمهعمر ۸۳۸ میلی ثانیه و ۹Li با نیمهعمر ۱۷۸ میلی ثانیهاست. دیگر ایزوتوپهای پرتوزا نیمهعمری کمتر از ۸٫۶ میلی ثانیه دارند. ناپایدارترین ایزوتوپ این عنصر ۴Li با نیمهعمر ۷٫۶ × ۱۰−۲۳ ثانیهاست که در آن پروتون پرتوزایی میکند.[۲۱]
۷Li یکی از عنصرهای بسیار کهن (یا دقیق تر بگوییم هستههای بسیار کهن) است که در جریان هستهزایی مهبانگ پدید آمدهاست. گمان آن میرود که مقدار اندکی از ۶Li و ۷Li در ستارهها پدید میآید اما به همان سرعتی که ایجاد میشود به همان سرعت، میسوزد و دوباره مصرف میشود.[۲۲] علاوه بر این احتمالا مقدار اندکی از ۶Li و۷Li در اثر بادهای خورشیدی و برخورد پرتوهای کیهانی با اتمهای سنگین تر و درنتیجه واپاشی ایزوتوپهایی مانند ۷Be و ۱۰Be پدید میآیند.[۲۳] هنگامی که لیتیم در جریان هستهزایی ستارهها پدید میآید دوباره سوخته و مصرف میشود. همچنین ۷Li در ستارههای کربنی هم میتواند تولید شود.[۲۴]
فرایندهای طبیعی گوناگونی میتوانند ایزوتوپهای لیتیم را تولید کنند.[۲۵] از جملهٔ آنها میتوان به پدیدهای شیمیایی هنگام ساخت کانیها، دگرگشت و داد و ستدهای یونی اشاره کرد. یون لیتیم در کانیهای رسی هشت وجهی جایگزین منیزیم و آهن میشود.
پیشینهٔ شناسایی

یوهان آگوست آرفودسن، کاشف لیتیم در ۱۸۱۷
شیمیدان برزیلی، خوزه بونیفاسیو جندراده نخستین کسی بود که کانی پتالیت (LiAlSi۴O۱۰) را شناسایی کرد. وی در سال ۱۸۰۰ میلادی در معدنی در یوتوی سوئد این کانی را پیدا کرد.[۲۶][۲۷][۲۸] هرچند، بر روی این کانی هیچ پژوهشی صورت نگرفت تا آنکه در سال ۱۸۱۷، شیمیدان سوئدی، یوهان آگوست آرفودسن که در آزمایشگاه یاکوب برسلیوس کار میکرد، دریافت که در این کانی عنصر تازهای وجود دارد.[۲۹][۳۰][۳۱] این عنصر تازه، ترکیبهایی همانند سدیم و پتاسیم را میپذیرفت تنها با این تفاوت که کربنات و هیدروکسید آن کمتر در آب حل میشد.[۳۲] برسلیوس این مادهٔ قلیایی را لیتیون (lithion/lithina) نام نهاد، برگرفته از واژهٔ یونانی لیتوس (λιθoς) به معنی «سنگ»؛ او به این دلیل این نام را برگزید تا نشان دهد که این عنصر را از یک کانی جامد بدست آوردهاست برخلاف پتاسیم که در میان خاکستر گیاهان شناسایی شد و همچنین در خون حیوانات هم به فراوانی یافت میشد. همچنین او به فلز درون ماده نام «لیتیم» را داد.[۱][۲۷][۳۱]
پس از چندی، آرفودسن نشان داد که این عنصر در کانیهای اسپودومن و لپیدولیت هم وجود دارد.[۲۷] در ۱۸۱۸ کریستین گملین نخستین کسی بود که دریافت نمکهای لیتیم شعله را به رنگ قرمز روشن در میآورند.[۲۷] هم گلمین و هم آرفودسن هر دو تلاش کردند تا لیتیم پالوده بدست آورند و عنصر را از نمکهایش جدا کنند که هر دو ناکام ماندند.[۲۷][۳۱][۳۳] تا سال ۱۸۲۱ کسی نتوانست لیتیم را پالوده بدست آورد تا اینکه شیمیدان انگلیسی، ویلیام توماس برند با کمک فرایند برقکافت بر روی لیتیم اکسید این عنصر را از ترکیبش بیرون کشید. برند نخستین کسی نبود که از برقکافت برای جداسازی بهره میبرد، پیش از او هم هامفری دیوی فرایندی همانند را برای جدا سازی فلزهای قلیایی پتاسیم و سدیم با موفقیت انجام داده بود.[۱۰][۳۳][۳۴][۳۵] همچنین برند توضیح داد که نمکهایی از لیتیم مانند کلرید و احتمالا لیتیا (لیتیم اکسید) دارای ۵۵٪ فلزند و برآورد کرد که وزن اتمی لیتیم 9.8 g/mol باشد (مقدار درست آن نزدیک به 6.94 g/mol است).[۳۶] در ۱۸۵۵ روبرت بونزن و آگوستس متیسن از راه برقکافت لیتیم کلرید مقدارهای بیشتری از این عنصر را جدا کردند.[۲۷] ادامهٔ تلاشها برای جداسازی بیشتر لیتیم از نمکهایش باعث دست یافتن به روش صنعتی این جداسازی در سال ۱۹۲۳ توسط یک تولیدکنندهٔ آلمانی به نام Metallgesellschaft AG شد. این تولیدکننده برای این هدف به برقکافت آمیختهای از لیتیم کلرید و پتاسیم کلرید پرداخت.[۲۷][۳۷]
نظرات شما عزیزان: